粘膜免疫とは、消化管関連リンパ組織(Gut-associated lymphoid tissues:GALT)または、鼻腔粘膜関連リンパ組織(Nasal-associated lymphoid tissue:NALT)を介した免疫応答のことである。これらの粘膜上皮は、外から入ってくる様々な外部抗原タンパクが最初に生体内に侵入する場であり、それゆえに粘膜のリンパ組織には、生体内でも最も多くのリンパ球が存在している。粘膜免疫では、これらのリンパ組織に目的のワクチン抗原だけを特異的に、しかも効率よく取り込ませることを目指している。粘膜免疫の利点として、副作用の減少、免疫方法の簡便化、コストの軽減などがあげられる。さらには、ワクチンになりうる抗原タンパクを植物に発現させた『食べるワクチン』への応用も期待することができる。
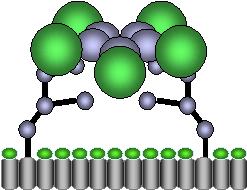
しかし粘膜免疫では、免疫原性が弱いことや、免疫寛容が誘導される恐れがあることから、目的の抗原タンパクと共に免疫アジュバントを用いる。コレラ毒素(cholera toxin:CT)のB subunit(CTB)もその一つであり、5量体を形成し、腸管などの細胞表面に多く散在するGM1-gangliosideに対して特異的に結合することが知られている。このCTBの性質を利用して、目的の抗原タンパクと融合させることで、免疫アジュバント効果を付与した。
免疫抗原として、狂犬病(rabies)ウイルスの唯一の膜表面上タンパクであるGタンパク(RaG)を用いた。狂犬病に対して有効な中和抗体を誘導するepitopeが立体構造を形成することから、昆虫細胞を用いてCTB-RaG融合タンパクを発現させ、マウスへの粘膜免疫実験を行っている。 |